Come l’antibiotico impatta sul microbiota intestinale? Focus on RIFAXIMINA
La classe di farmaci più utilizzata al mondo è quella degli antibiotici, pietra miliare della terapia medica. Se da un lato l’effetto anti-patogeno è voluto, l’impatto che hanno però sul microbiota intestinale è oggetto di studio e spesso associato a diverse malattie croniche come asma, allergie, obesità, diabete e malattie infiammatorie intestinali.
La recente review The effect of antibiotics on the composition of the intestinal microbiota evidenzia come le diverse classi di antibiotici impattino sul microbiota intestinale. Conoscere i cambiamenti del consorzio microbico intestinale in base all’antibiotico utilizzato, getta le basi per possibili e mirati interventi probiotici e dietetici per ripristinarne l’eubiosi riducendo questo “danno collaterale”.
L’effetto degli antibiotici sul microbiota intestinale varia al variare della molecola utilizzata, probabilmente in base al suo spettro d’azione (ristretto vs ampio), via di somministrazione, farmacocinetica e farmacodinamica. Molecole ampiamente utilizzate come Amoxicillina, Cefalosporine e Macrolidi, dopo una singola terapia apportano cambiamenti al microbiota intestinale per oltre 30 giorni, mentre Chinoloni e Clindamicina provocare disbiosi per quasi 2 anni. Tra tutti gli antibiotici analizzati, la Rifaximina sembrerebbe la molecola meno dannosa per il consorzio microbico intestinale, purtroppo però, in tutti i casi si assiste sempre ad una riduzione dei Bifidobatteri che risultano i più sensibili agli antibiotici.
Quali le principali conseguenze sul microbiota dopo antibiotico terapia?
Anche se somministrato per un tempo molto limitato, l’antibiotico ha un impatto importante sul microbiota intestinale. Nello studio pubblicato su Plos-One Short-term effect of antibiotics on Human gut microbiota i ricercatori hanno appurato che già dopo un singolo ciclo terapico di antibiotico la biodiversità del microbiota intestinale si riduceva del 25%.
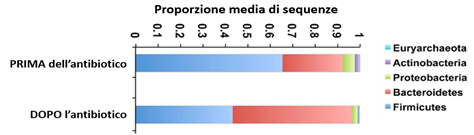
Paradossalmente, dopo l’uso dell’antibiotico il numero di batteri intestinali aumentava leggermente ma a favore di specie Gram-negative, raggiungendo valori anche doppi da quelli di partenza.
Questo rimodellamento microbico a favore dei batteri Gram-negativi suggerisce che la riduzione di batteri sensibili agli antibiotici fornisce spazio a ceppi maggiormente resistenti che ne occupano la nicchia ecologica rimasta vuota.
Tra tutti, i bifidobatteri e i lattobacilli sono i primi a subire drastiche riduzioni anche in seguito a una singola dose di antibiotico.
Quali le conseguenze sul microbiota intestinale dopo l’uso della Rifaximina?
La Rifaximina è un antibiotico ampiamente utilizzato per i suoi effetti confinati all’intestino. Diversi lavori dimostrano come essa abbia un ottimo effetto antibatterico a livello intestinale, con un impatto sul microbiota non paragonabile a quello di altri farmaci della stessa classe. Il danno provocato sul microbiota intestinale è molto contenuto e laddove utilizzata per un breve periodo, il consorzio microbico riesce a recuperare la disbiosi in circa 7-10 giorni. Pur avendo caratteristiche uniche, nell’articolo Utility of the Nonabsorbed (<0.4%) Antibiotic Rifaximin in Gastroenterology and Hepatology viene valutata la MIC50 e la MIC90 su determinate classi batteriche.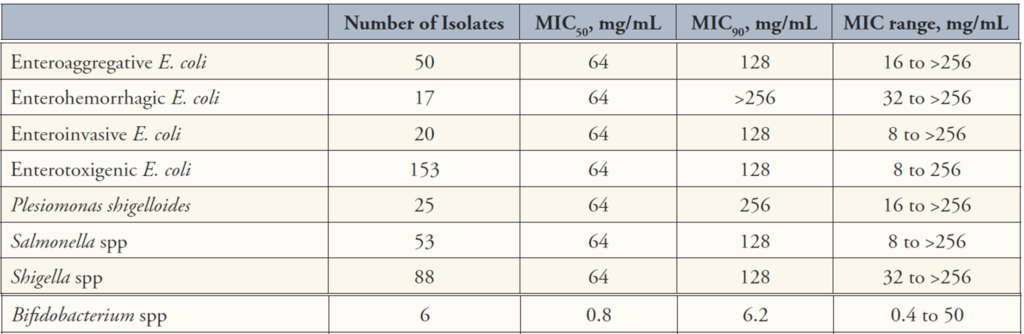
Seppure con un’incidenza minore, l’attività antibiotica d. ella Rifaximina è rilevabile anche su batteri non patogeni come il genere Bifidobacterium spp., effetto ancora più evidente per cicli terapeutici consecutivi.
Anche Akkermansia muciniphila, specie batterica che il compito di ridurre la permeabilità intestinale proteggendo la mucosa, viene drasticamente ridotta dopo un singolo ciclo di Rifaximina, così come mostrato nel recente lavoro Impact of treatments on fecal microbiota and fecal metabolome in symptomatic uncomplicated diverticular disease of the colon: a pilot studyRispetto ad una riduzione del 25% della biodiversità del microbiota intestinale mostrato per altri antibiotici, la Rifaximina ha una riduzione di circa il 12% della diversità intestinale che si verifica dopo sole 2 settimane di utilizzo.
Risulta quindi evidente come la conoscenza delle esatte conseguenze disbiotiche dovute all’uso di antibiotici ponga le basi per interventi mirati a ridurre tale effetto tramite la supplementazione di batteri probiotici e opportuni interventi dietetici.